神經(jīng)元是神經(jīng)系統(tǒng)的解剖和功能單位,調(diào)節(jié)生命功能和高級(jí)功能。 在體內(nèi)極少數(shù)不再生的細(xì)胞中�,盡管它們的完整性受到了許多威脅,但這些細(xì)胞必須保持健康���,同時(shí)仍能正常運(yùn)作����。 雜志上的一篇新研究論文 EMBO Reports 描述了 DNA 損傷如何影響神經(jīng)健康和功能�。
介紹
神經(jīng)元具有高效的機(jī)制來(lái)抵抗基本遺傳密碼的變化,稱為 DNA 損傷反應(yīng) (DDR) 途徑�。 如果在這些途徑中發(fā)生功能喪失突變,它們?cè)馐艿膿p失最大�,因?yàn)樗鼈儓?zhí)行的許多任務(wù)除了需要轉(zhuǎn)錄準(zhǔn)確性外,還消耗大量能量���。
如果這些通路在需要時(shí)無(wú)法發(fā)揮作用���,有害的基因組重排、轉(zhuǎn)錄通路的失調(diào)和受損基因組位點(diǎn)的積累會(huì)導(dǎo)致對(duì)神經(jīng)元的毒性累積�����。 最終,這些導(dǎo)致細(xì)胞凋亡��、衰老或不受調(diào)節(jié)的細(xì)胞分裂����、衰老和退化的跡象。
神經(jīng)退行性疾病是無(wú)法存活的神經(jīng)元的結(jié)果����,從長(zhǎng)遠(yuǎn)來(lái)看,這反過(guò)來(lái)會(huì)導(dǎo)致記憶力減退����、運(yùn)動(dòng)障礙和獨(dú)立性喪失。 與神經(jīng)退行性變相關(guān)的疾病在美國(guó)的死亡原因中排名第三���,在世界范圍內(nèi)排名第五����。
最近的研究表明��,大量的 DDR 通路在防止基因組 DNA
因外部損傷和體內(nèi)毒性過(guò)程造成的損傷方面發(fā)揮著重要作用�。
每條通路都會(huì)對(duì)特定類型的損傷做出反應(yīng)���,使用自己的級(jí)聯(lián)酶和修復(fù)蛋白首先檢測(cè)損傷,然后通過(guò)核酸酶活性修復(fù)或切除受損位點(diǎn)�,最后構(gòu)建新的 DNA
以填補(bǔ)缺口聚合酶的幫助。 然后使用連接酶將 DNA 鏈的切割末端密封在一起����。
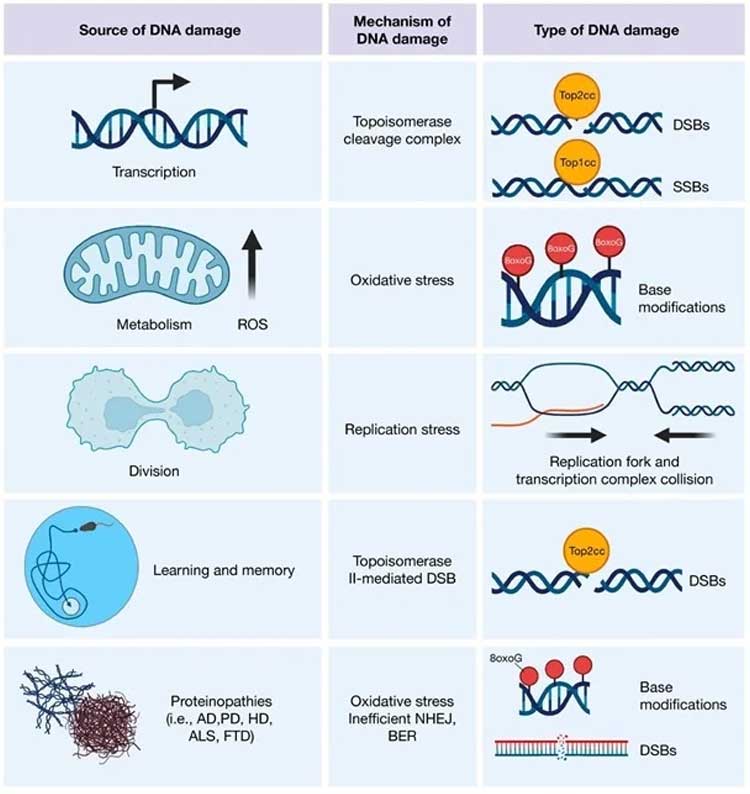
大腦中
DNA 損傷的來(lái)源 轉(zhuǎn)錄活動(dòng)可導(dǎo)致拓?fù)洚悩?gòu)酶裂解復(fù)合物,從而根據(jù)所討論的拓?fù)洚悩?gòu)酶誘導(dǎo) SSB 或 DSB��。 此外����,線粒體的代謝活動(dòng)會(huì)產(chǎn)生
ROS����,它可以通過(guò)氧化修飾使 DNA 堿基形成疤痕。 雖然在成人大腦中不太常見(jiàn)�,但細(xì)胞分裂也是 DNA 損傷的來(lái)源。
增殖增加了復(fù)制叉和轉(zhuǎn)錄復(fù)合物碰撞的機(jī)會(huì)���,從而誘導(dǎo)了 DSB�����。 在發(fā)育中的大腦中�����,這對(duì) NPC 來(lái)說(shuō)是一種特殊的風(fēng)險(xiǎn)���,NPC
的長(zhǎng)基因(這些碰撞最有可能發(fā)生的地方)易位增加���,這對(duì)神經(jīng)元功能很重要。
認(rèn)知要求高的任務(wù)會(huì)招募特定的神經(jīng)元集合�����,其可塑性高度依賴于即時(shí)的早期基因轉(zhuǎn)錄�。 因此,神經(jīng)元產(chǎn)生拓?fù)洚悩?gòu)酶 II 介導(dǎo)的 DSB
以響應(yīng)學(xué)習(xí)和記憶�����。 最后��,還發(fā)現(xiàn)導(dǎo)致各種神經(jīng)退行性疾病的蛋白質(zhì)在 DNA 損傷檢測(cè)和修復(fù)中發(fā)揮作用�����。
單股斷裂
大多數(shù)基因組 DNA 損傷是由活性氧 (ROS) 介導(dǎo)的,它會(huì)導(dǎo)致單鏈斷裂 (SSB)��。 該途徑主要發(fā)生在神經(jīng)系統(tǒng)中��,因?yàn)樵撓到y(tǒng)內(nèi)對(duì)線粒體呼吸的需求很高����,占人體總攝氧量的五分之一。 線粒體代謝可能引起代謝活動(dòng)����。
ROS 誘導(dǎo)的 SSB 存在直接和間接機(jī)制。
對(duì)于后者�����,由于需要修復(fù)有毒的 DNA 修飾�,例如非常常見(jiàn)的 8-oxo-7,8-二氫鳥(niǎo)嘌呤
(8oxoG)���,它會(huì)破壞基因轉(zhuǎn)錄過(guò)程����,并且如果修復(fù)錯(cuò)誤會(huì)導(dǎo)致突變����,加速大腦衰老和疾病�。
這是一類稱為非大堿基修飾的修飾的一部分�,通過(guò)堿基切除修復(fù) (BER) 修復(fù),包括切除�����,以及短補(bǔ)丁或長(zhǎng)補(bǔ)丁 SSB 修復(fù)(分別為 sp-或
lp-SSBR)��。
紫外線誘導(dǎo)的 DNA
損傷是大面積損傷的形式�,這些損傷會(huì)在空間上扭曲 DNA 螺旋。 這通過(guò)兩種途徑之一啟動(dòng)檢測(cè)和核苷酸切除修復(fù) (NER)���。 直接 SSB
的第三種方法是通過(guò)終止拓?fù)洚悩?gòu)酶 I (TOP1) 激活�,導(dǎo)致 TOP1 DNA 切割復(fù)合物 (Top1cc) 的形成�����。
在存在氧化性 DNA 損傷的情況下�����,Top1cc 無(wú)法解決,這意味著這是一種特別有毒的神經(jīng)元損傷形式���。 一種稱為脊髓小腦性共濟(jì)失調(diào)伴軸突神經(jīng)病變 (SCAN1) 的遺傳病是由于缺乏解決這種損傷的 SSB 修復(fù)酶�。
雙鏈斷裂
雙鏈斷裂 (DSB) 可能比 SSB 更不常見(jiàn)��,但毒性可能更大���,盡管它們?cè)诶绠a(chǎn)生廣泛的 T 細(xì)胞 受體和抗體多樣性以及減數(shù)分裂重組中發(fā)揮生理作用�。 在積極復(fù)制的細(xì)胞中���,DSB 更常見(jiàn)���,可能是因?yàn)閺?fù)制叉與轉(zhuǎn)錄復(fù)合物發(fā)生碰撞。
然而�,大多數(shù) DSB 是由于拓?fù)洚悩?gòu)酶裂解復(fù)合物的轉(zhuǎn)錄過(guò)程而發(fā)生的。 由于酪氨酰-DNA 磷酸二酯酶 2 (TDP2) 酶的缺失�,應(yīng)立即分解這些復(fù)合物的拓?fù)洚悩?gòu)酶 II (TOP2) 切割復(fù)合物旨在緩解扭轉(zhuǎn)并暴露某些轉(zhuǎn)錄基因�,從而導(dǎo)致 DSB 產(chǎn)生。
DSB 修復(fù)通過(guò)同源末端連接 (NHEJ) 和同源重組
(HR) 進(jìn)行����。 第二種方法使用姐妹染色單體作為模板合成 DNA 修復(fù)裂口,因此沒(méi)有錯(cuò)誤,但只能發(fā)生在復(fù)制細(xì)胞或 S 期之后����。
因此,大多數(shù)有絲分裂后細(xì)胞的主要 DSB 修復(fù)途徑是 NHEJ����。 單鏈退火 (SSA) 是一種替代途徑,但與 NHEJ 一樣����,與 HR
相比更容易出錯(cuò)。
功能中斷可能會(huì)導(dǎo)致以后的功能障礙
DNA
斷裂可能在神經(jīng)元活動(dòng)中具有生理作用�,但當(dāng)它們發(fā)生在神經(jīng)元調(diào)節(jié)序列中時(shí),它們可能會(huì)誘導(dǎo)突變和易位�,從而導(dǎo)致影響突觸信號(hào)傳導(dǎo)的轉(zhuǎn)錄途徑的擾動(dòng)。
一些 DNA 修復(fù)繪圖技術(shù)正在開(kāi)發(fā)或已經(jīng)在使用����,并證實(shí)了這一假設(shè)。 聚 (ADP-核糖) 聚合酶 1 (PARP1)
和突變的共濟(jì)失調(diào)毛細(xì)血管擴(kuò)張癥 (ATM) 是 SSB 和 DSB 的兩個(gè)主要傳感器�����。
DNA修復(fù)綜合征引起的神經(jīng)系統(tǒng)疾病
現(xiàn)在已知許多神經(jīng)系統(tǒng)疾病是由可遺傳的 DNA 損傷疾病引起的�����,導(dǎo)致年齡相關(guān)或神經(jīng)發(fā)育后遺癥。 這些包括導(dǎo)致功能喪失和純粹表現(xiàn)為神經(jīng)退行性疾病的 SSBR 蛋白突變����,包括 1 型和 4 型動(dòng)眼神經(jīng)失用癥(AOA1、AOA4)的共濟(jì)失調(diào)�����。
SSBs 也可以形成 DSBs����,在神經(jīng)元中,不能被 HR
修復(fù)�����。 有缺陷的 SSBR 可通過(guò)多種機(jī)制引發(fā)神經(jīng)毒性�。 一方面,沒(méi)有修復(fù)蛋白 XRCC1��,PARP1
變得過(guò)度活躍��,導(dǎo)致聚(ADP-核糖)的積累���。 這反過(guò)來(lái)會(huì)耗盡細(xì)胞中的 NAD+/ATP���,并通過(guò) Parthanatos 途徑導(dǎo)致細(xì)胞死亡。
已經(jīng)闡明了 PARP1 誘導(dǎo)的神經(jīng)毒性的幾種機(jī)制�,包括 DNA 修復(fù)的失調(diào)、轉(zhuǎn)錄的抑制以及 SSB 在調(diào)節(jié)神經(jīng)元活動(dòng)的增強(qiáng)子位點(diǎn)的積累��。
由于 ATM 激酶的突變����,DSBR
突變還可能導(dǎo)致神經(jīng)系統(tǒng)綜合征,例如共濟(jì)失調(diào)毛細(xì)血管擴(kuò)張癥���。 與單獨(dú)的 ATM
基因突變不同��,多重突變可能導(dǎo)致神經(jīng)元基因組不穩(wěn)定的閾值降低����,從而導(dǎo)致神經(jīng)結(jié)構(gòu)和功能缺陷�。
這可能是因?yàn)樾∧X浦肯野細(xì)胞具有開(kāi)放的染色質(zhì)片段,這些染色質(zhì)對(duì)某些類型的 DNA
破壞修復(fù)機(jī)制的異常敏感���,導(dǎo)致浦肯野細(xì)胞基因表達(dá)不足以及特征性小腦萎縮和共濟(jì)失調(diào)�����。
神經(jīng)退行性疾病和 DNA 損傷
氧化損傷見(jiàn)于衰老和神經(jīng)變性患者的腦組織�����,例如帕金森病
(PD) 或阿爾茨海默病 (AD)���。 這與 8oxoG 隨著年齡的增長(zhǎng)而增加有關(guān)��,組蛋白去乙?����;?HDAC1 減輕了這一點(diǎn)�����。 單核苷酸變異
(SNV) 可能是高 8oxoG 水平的結(jié)果���,這會(huì)在許多水平上干擾基因轉(zhuǎn)錄。
這包括抑制轉(zhuǎn)錄因子結(jié)合�、異常 BER 和基因啟動(dòng)子的甲基化。
由此產(chǎn)生的 SNV 積累可能導(dǎo)致有絲分裂后神經(jīng)元的基因組多樣性�����,導(dǎo)致上述條件下的神經(jīng)元功能障礙�。 在亨廷頓氏病 (HD)
中,標(biāo)志性的年齡依賴性 CAG 擴(kuò)增導(dǎo)致紋狀體中的毒性變化�����,這是由于 DNA 修復(fù)蛋白檢測(cè)到重復(fù)序列中的氧化或錯(cuò)配堿基���,然后觸發(fā)不必要的修復(fù)�����。
DNA維持基因中的單核苷酸多態(tài)性(SNP)可以降低HD的發(fā)病年齡�,從而影響其嚴(yán)重程度���。
重要的是���,在所有這些情況下,SSB 和 DSB 都處于高水平�,并且在疾病過(guò)程中伴隨著重要的標(biāo)志物,例如認(rèn)知障礙�。 這表明 DNA 鏈斷裂可能導(dǎo)致疾病進(jìn)展��。 許多由異常蛋白質(zhì)生成引起的神經(jīng)退行性疾病的生物標(biāo)志物基因都參與了 DDR 通路��。
這些和類似的發(fā)現(xiàn)“ 已經(jīng)確定 DNA 斷裂是神經(jīng)退行性疾病的一種機(jī)制 ����?�!?
此外���,對(duì)有絲分裂后神經(jīng)元中 DNA
斷裂的全基因組研究表明�,這種斷裂在影響突觸信號(hào)傳導(dǎo)和神經(jīng)元功能的調(diào)節(jié)區(qū)域的位置是它們對(duì)神經(jīng)系統(tǒng)產(chǎn)生毒性作用的主要原因�����。
也就是說(shuō)�,盡管它們具有功能相關(guān)性,但如果修復(fù)不當(dāng)�����,這些斷裂可能會(huì)通過(guò)錯(cuò)誤的易位和突變導(dǎo)致基因組易位����。
神經(jīng)炎癥
神經(jīng)炎癥是神經(jīng)退行性疾病的另一個(gè)關(guān)鍵特征�,是神經(jīng)毒性的主要介質(zhì)����。 AD 的許多風(fēng)險(xiǎn)基因?qū)嶋H上會(huì)影響小膠質(zhì)細(xì)胞的功能,這些基因是大腦中的巨噬細(xì)胞�,與神經(jīng)炎癥有關(guān)�。 衰老可能是這種炎癥和神經(jīng)退行性變的驅(qū)動(dòng)因素,類似的信號(hào)可能來(lái)自 DNA 損傷的神經(jīng)元�����。
此類信號(hào)可能通過(guò)多種來(lái)源產(chǎn)生��,包括通過(guò)衰老和 DNA 損傷(通過(guò) DDR 途徑)激活炎癥信號(hào)���,以及由 核酸 傳感器環(huán) GMP-AMP(cGAMP) ) 合酶 (cGAS)�����,可激活 IFN 基因刺激物 (STING)�����。 這會(huì)引發(fā)多級(jí)炎癥反應(yīng)�����。
細(xì)胞溶質(zhì) DNA 還激活 TLR9(Toll 樣受體 9)或 NLRP3 炎性體�,所有這些都會(huì)導(dǎo)致神經(jīng)炎癥。
分子細(xì)胞生物學(xué)實(shí)驗(yàn)
輝駿實(shí)力












 實(shí)驗(yàn)熱線:4006991663
實(shí)驗(yàn)熱線:4006991663